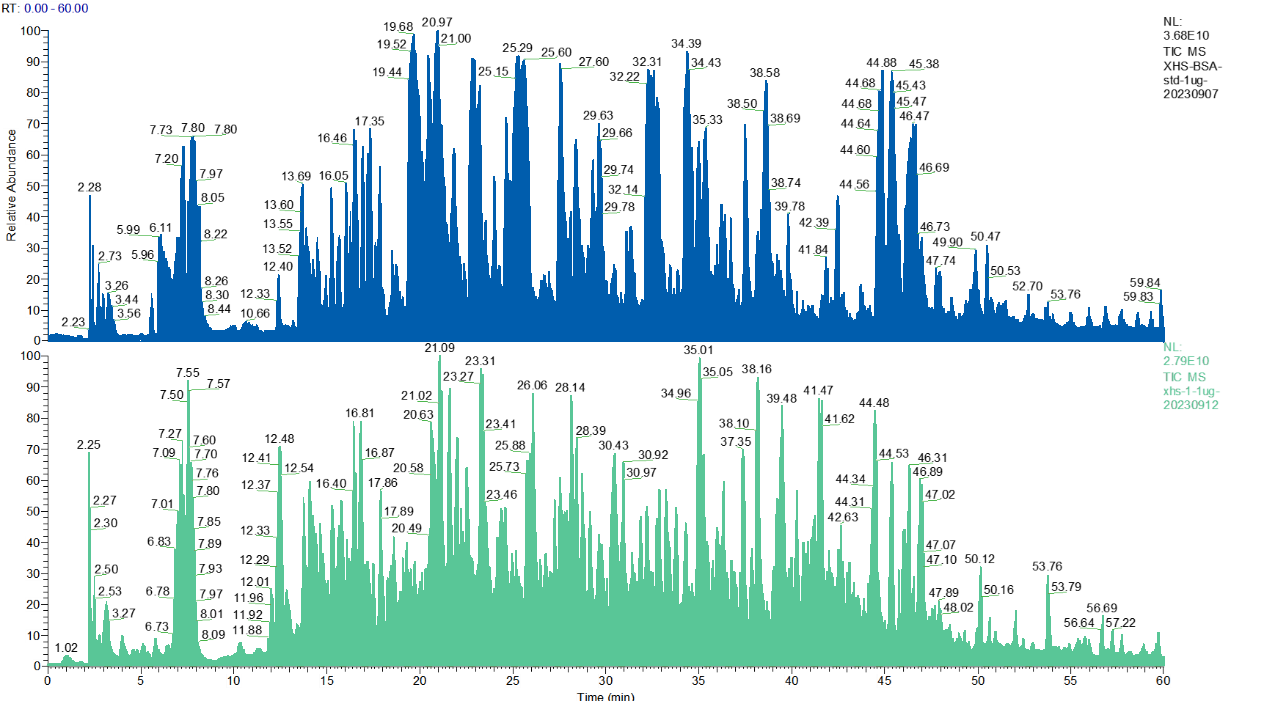
재조합 단백질은 주로 세균, 효모, 포유류, 곤충 또는 식물 세포주와 같은 숙주 세포에서 발현된다. 생물 생산 과정 동안, 이들 숙주 세포는 또한 정상적인 세포 기능에 필요한 부산물 단백질을 생산한다. 세포가 세포 사멸, 사망 및 용해됨에 따라, 이들 부산물 단백질은 세포 배양 배지로 방출된다. 결과적으로,잔류 숙주 세포 단백질임상 안전성과 효능에 영향을 줄 수있는 중요한 공정 관련 불순물이됩니다. 미국 약전은 HCP 잔기 수준이 1-100 ng/mg의 범위가되어야한다고 규정하고 있습니다.
ELISA 분석은 일부 제한에도 불구하고 HCP 정량화를 위한 약리 방법이다. 예를 들어, ELISA 키트의 항체 커버리지는 단지 약 50%-80%, 이는 모든 HCP 유형을 커버할 수 없음을 의미한다. 또한, ELISA는 HCP의 총량만을 측정할 수 있고, 개별 HCP의 유형 및 양에 대한 정보를 제공할 수 없다. 따라서 업계 전문가들은 직교 방법으로 HCP의 정확한 식별 및 정량적 분석을 위해 질량 분석법을 사용하고 추천.
1. 바이오 프로세스 최적화
HCP 제거의 단계적 효율을 분석하여 최적의 경로를 확인하기 위해 서로 다른 경로로부터의 공정 내 샘플의 비교 연구를 수행한다. ELISA는 총 HCP 함량만을 검출할 수 있기 때문에, 함량이 높지만 면역원성이 낮은 일부 HCP (항체에 의해 인식되지 않음) 는 효과적으로 모니터링될 수 없다. 따라서 보다 정확한 모니터링을 위해 공정 개발 중에 질량 분석 데이터를 사용하는 것이 좋습니다.
2. 최종 제품의 HCP 분석
바이오프로세싱의 안정성을 평가하기 위해 상이한 배치로부터의 약물 물질의 비교 분석이 수행된다. 이 분석은 ELISA 데이터와 결합하여 잔류 HCP 불순물을 추가로 평가하고 임상 위험을 감소시킵니다.